Насыщенная липидами клеточная стенка микобактерии обусловливает их кислотоустойчивость. Существует более пятидесяти видов микобактерии, большинство из которых присутствует в окружающей среде и не представляет опасности для человека.
Эпидемиология и патогенез туберкулеза (Mycobacterium tuberculosis)
Основной путь передачи туберкул ёза - воздушно-капельный. Лёгкие являются первым органом, поражаемом при туберкулёзе. В месте проникновения возбудителя формируется воспалительный очаг (первичный комплекс), из которого инфекция может распространиться по всему организму (милиарное распространение). Заболевание может неожиданно разрешиться либо перейти в локализованный процесс (например, менингит).
Устойчивость к туберкулёзу обеспечивает Т-клеточное звено иммунитета. При его нарушении болезнь может рецидивировать (предполагаемый риск составляет 10%). Яркую клиническую картину заболевания чаще обнаруживают у пациентов со сниженным иммунитетом (например, у больных с ВИЧ-инфекцией).
Фагоцитируются макрофагами, но не инактивируются фаголизосомами, а размножаются в цитоплазме клеток. Выраженный иммунный ответ приводит к локальному разрушению тканей (образование полостей в лёгких - каверн) и возникновению симптомов, обусловленных цитокин-индуцированной системной воспалительной реакцией (лихорадка, потеря массы тела).
В качестве факторов вирулентности выступает большое количество антигенов, в том числе липоарабиноманнан (стимулятор цитокинов) и супероксиддисмутаза (обеспечивает выживаемость внутри макрофагов).
Клинические признаки туберкулеза
Возбудитель может поражать любой орган: он имитирует как воспалительные заболевания, так и злокачественные новообразования. Симптомы туберкулёза лёгких - хронический кашель, кровохаркание, лихорадка, потеря массы тела, рецидивирующая бактериальная пневмония. При отсутствии лечения болезнь переходит в хроническую форму, характеризующуюся постепенным ухудшением состояния.
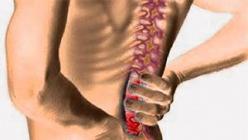
При туберкулёзном менингите отмечают повышение температуры, помутнение сознания, при поражении почек - лихорадку, потерю массы тела, а также признаки локальной инфекции, осложнённой фиброзом мочеточников и гидронефрозом. Прогрессирование туберкулёза костей, обычно поражающего пояснично-крестцовый отдел позвоночника, характеризуется признаками вертебрального коллапса и сдавления нервов.
Кроме того, гной из очага инфекции может проникать под оболочку поясничной мышцы, в результате чего возникает паховый абсцесс. Поражение крупных суставов приводит к артриту и разрушению суставной ткани. При абдоминальной инфекции наблюдают брыжеечную лимфаденопатию, хронический перитонит, а также лихорадку, потерю массы тела, асцит, признаки нарушения всасывания в кишечнике. Диссеминированная (милиарная) инфекция может протекать без симптомов поражения лёгких.
Микобактерии туберкулезаЛабораторная диагностика туберкулеза (Mycobacterium tuberculosis)
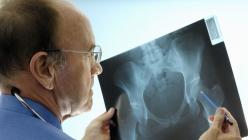
Культивирование на средах, обогащенных липидами (яичные среды), или с добавлением малахитового зелёного (среда Левенштейна-Йенсена) для подавления роста других бактерий. Препарат окрашивают по методу Циля-Нильсена.
Определение чувствительности штаммов на скошенной питательной среде Левенштейна-Йенсена.
Молекулярно-генетические методы (помогает уточнить наличие гена ргоВ, идентифицировать туберкулёзный антигенный комплекс и определить устойчивость к рифампицину).
Типирование Mycobacterium tuberculosis с помощью анализа полиморфизма длины рестрикционных фрагментов.
Измерение уровня цитокинов периферической крови, продуцируемых моноцитами (для диагностики остроты процесса).
Лечение и профилактика туберкулеза
Для лечения туберкулёза лёгких применяют этамбутол в комплексе с пиразинамидом (в первые 2 мес) и рифампицин и изониазид (на протяжении 6 мес). При поражении других органов используют такую же схему лечения, основанную на способности лекарственного препарата проникать в различные ткани (например, в спинномозговую жидкость). В последнее время всё чаще выделяют мультирезистентные штаммы возбудителя туберкулёза.
Вероятность их обнаружения зависит от числа случаев неполного излечения, уровня жизни и др. В этом случае для лечения используют препараты второй линии: аминогликозиды, фторхинолоны, этионамид или циклосерин (после обязательного определения чувствительности возбудителя к антибиотикам).
Вакцинация аттенуированными (ослабленными) штаммами (вакцина для профилактики туберкулёза, синоним - вакцина Кальметт-Герена, БЦЖ) позволяет избежать милиарного распространения инфекции, но клинические исследования в некоторых странах не подтвердили её эффективности. Пациентам с высоким риском развития туберкулёза назначают профилактическое лечение рифампицином и изониазидом, а лицам с ВИЧ-инфекцией рекомендован приём рифабутина или кларитромицина в течение длительного времени.
 Микобактерии лепры
Микобактерии лепры
Инфекция вызванная Mycobacterium leprae - Лепра
Возбудителя лепры (проказы) до настоящего времени не удалось культивировать на искусственных питательных средах.
Mycobacterium leprae
вызывает поражение периферических нервов, сопровождаемое нарушением болевой чувствительности. Разрушение и деформация суставов и фаланг пальцев делают пациентов физически недееспособными. Итог заболевания индивидуален и зависит от иммунного ответа. В настоящее время выделяют три типа иммунного ответа при лепре:
туберкулоидный (превалирует Thl-ответ);
лепроматозный (преобладает Тh2-ответ);
пограничный.
При туберкулоидном типе инфекции у пациентов развивается стойкий клеточный иммунитет, возникает большое количество гранулём, трофические поражения нервов. В тканях обнаруживают небольшое количество бактерий. Для лепроматозного типа характерен слабый клеточный иммунитет, отсутствие гранулём и генерализованная инфекция (леонтиаз, депигментация и нарушение чувствительности).
Диагноз основан на результатах микроскопического исследования препаратов поражённой кожи (окраска по Цилю-Нильсену) и биоптатов кожных покровов гистологического исследования. Для лечения применяют рифампицин, дапсон и клофазимин, эффективные на ранних стадиях заболевания, но неспособные препятствовать повреждению нервов и деформации конечностей, при возникновении которых необходимо хирургическое вмешательство.
Микобактерии не вызывающие туберкулез
Различные виды микобактерий могут вызывать локализованные или диссеминированные заболевания у лиц со сниженным иммунитетом. Некоторые из них могут инфицировать имплантируемые ткани.
Mycobacterium avium . В состав комплекса входят Mycobacterium avium, M. intracellular и М. scrofulaceum. Некоторые из них поражают птиц, других животных, являясь санрофитами окружающей среды. Их считают наиболее распространённой причиной микобактериального лимфаденита у детей, остеомиелита у пациентов со сниженным иммунитетом и пневмонии у лиц пожилого возраста. При прогрессирующей ВИЧ-инфекции эти микроорганизмы способны вызывать диссеминированные инфекции и бактериемию.
Возбудители из авиум-внутриклеточного комплекса устойчивы к действию большинства противотуберкулёзных препаратов, поэтому для лечения инфекций, вызванных ими, применяют методы комплексной терапии с использованием рифабутина, кларитромицина и этамбутола. При развитии лимфаденита иногда требуется хирургическое вмешательство.
Mycobacterium kansasi, M. Malmoense, M. Xenopi . Вызывают вялотекущую инфекцию лёгких, похожую на туберкулёз, у пациентов с хроническими заболеваниями лёгких (бронхоэктазией, силикозом, хронической обструктивной болезнью лёгких). Начальную терапию осуществляют с помощью стандартных препаратов после определения чувствительности микроорганизмов к антибиотикам.
Mycobacterium marinum, М. ulcerans . Mycobacterium marinum вызывают хронические гранулематозные инфекции кожи. Возбудитель обитает в реках, запущенных бассейнах и неухоженных садках для рыбы. Заболеванию свойственно возникновение множественных гнойничковых очагов, покрытых твёрдой коркой. Инфекции, вызванные М. ulcerans, распространены в сельскохозяйственных зонах Африки и Австралии. Бактерии обычно поражают нижние конечности, при этом обнаруживают папулёзные очаги, сопровождаемые изъязвлением и глубоким повреждением тканей (включая костную).
Атипичные (нетуберкулезные, нелепрозные) микобактерии относятся к семейству Mycobacteriaceae и отличаются от М. tuberculosis по потребности в питательных веществах, способности образовывать пигменты, ферментной активности и чувствительности к противотуберкулезным средствам. Кроме того, М. tuberculosis, как правило, распространяется от человека к человеку, а заражение атипичными микобактериями происходит при контакте с окружающей средой.
Эпидемиология
Атипичные микобактерии есть повсеместно и служат сапрофитными обитателями почвы и воды, возбудителями инфекций у свиней, птиц и крупного рогатого скота, кроме того, микобактерии могут входить в состав нормальной микрофлоры глотки человека.
У некоторых атипичных микобактерий есть четкие экологические ниши, которые помогают объяснить особенности их передачи. Так, естественным резервуаром для М. marinum служат рыбы и прочие холоднокровные животные, а инфекция развивается после травм, произошедших в воде. М. fortuitum и М. chelonae - повсеместно распространенные представители больничной микрофлоры, поэтому они вызывают больничные вспышки раневой инфекции либо инфекции, связанной с венозными катетерами. М. ulcerans выделяется исключительно из воды и почвы джунглей; она служит возбудителем хронических инфекций кожи в тропиках. Микобактерии комплекса М. avium в изобилии обнаруживаются в воде, почве и аэрозолях, образующихся из кислой коричневой воды болот на юго- востоке США. В сельской местности этого региона бессимптомные инфекции, вызванные комплексом М. avium, к моменту вступления во взрослую жизнь переносят около 70 % людей.
У детей атипичные микобактерии редко становятся возбудителями инфекций (исключение - шейный лимфаденит). Инфекции атипичных микобактерий (особенно комплексом М. avium), - наиболее частые инфекции, возникающие в терминальный период .
Патогенез
Гистологически очаги инфекции, вызванной М. tuberculosis и атипичными микобактериями, часто неразличимы. Классическим морфологическим проявлением в обоих случаях служит гранулема с казеозным некрозом. Но для атипичных микобактерий более характерны гранулемы без казеозного некроза, плохо отграниченные (без палисадообразных структур), неправильной формы или ползучие. Гранулемы могут отсутствовать, тогда обнаруживаются лишь хронические воспалительные изменения. У больных СПИДом с инфекцией атипичными микобактериями, воспалительная реакция обычно слабо выражена, а в тканях имеется большое количество гистиоцитов, заполненных кислотоустойчивыми палочками.
Клинические проявления
У детей самым частым проявлением инфекций атипичных микобактерий служит лимфаденит передних шейных или поднижнечелюстных лимфатических узлов; изредка вовлекаются околоушные, задние шейные, подмышечные и паховые лимфатические узлы. Лимфаденит в основном наблюдается у детей 1-5 лет, которые имеют привычку класть в рот предметы, загрязненные почвой, пылью или непроточной водой. Причиной обращения к врачу служит увеличение (сравнительно быстрое или медленное) лимфатического узла или группы тесно расположенных лимфатических узлов с одной стороны; системные проявления обычно отсутствуют. Пораженные лимфоузлы больше 1,5 см, плотные, безболезненные, подвижные, кожа не гиперемирована. Без лечения лимфатические узлы в некоторых случаях могут вернуться к исходным размерам, однако чаще всего через несколько недель они нагнаиваются. В центре лимфатического узла появляется флюктуация, а кожа над ним становится гиперемированной и истончается. Вскоре лимфатический узел вскрывается и образуется кожный свищ, не заживающий месяцами или даже годами, - картина на этой стадии напоминает классический туберкулезный лимфаденит. Возбудителем приблизительно 80% лимфаденитов у детей, вызванных атипичными микобактериями, является комплекс М. avium. Большинство остальных случаев вызвано М. scrofulaceum и М. kansasii. К редким возбудителям относятся М. xenopi, М. malmoense, М. haemophilumи М. szulgai.
Кожные инфекции атипичных микобактерий встречаются редко. Обычно инфекция развивается вслед за попаданием в кожную рану (мелкая ссадина на локте, колене или ступне у пловцов; ссадины на кистях рук гранулема аквариумистов) воды, загрязненной М. marinum. В течение нескольких недель на месте травмы возникает одиночный узелок - гранулема купальщиков. Обычно узелок безболезненный, увеличивается и через 3-5 нед. превращается в бляшку с изъязвленной или бородавчатой поверхностью (сходная картина наблюдается при туберкулезе кожи). Иногда картина напоминает споротрихоз: вблизи первичного узелка возникает сателлитные, которые располагаются по ходу поверхностных лимфатических сосудов. Лимфаденопатия, как правило, отсутствует. Хотя в большинстве случаев инфекция ограничивается кожей, внедрение в более глубокие ткани может привести к тендовагиниту, бурситу, остеомиелиту или артриту.
М. ulcerans тоже вызывает инфекции кожи у детей, живущих в тропиках (Африка, Австралия, Азия и Южная Америка). Инфекция возникает после внедрения возбудителя в кожу и проявляется безболезненным гиперемированным узелком (чаще всего на ногах), в центре которого возникает некроз, а затем и язва. Заболевание называется язвой Бурули (по названию региона в Уганде, где регистрируется большинство случаев). Язва характеризуется подрытыми краями, медленным увеличением и может привести к обширному разрушению мягких тканей и осложниться вторичной бактериальной инфекцией. В течение 6-9 мес. язва может зажить или продолжать увеличиваться, что сопровождается деформациями и контрактурами.
М. fortuitum, М. chelonae и М. abscessus редко вызывают инфекции у детей. Местом внедрения возбудителя обычно служат колотые раны или мелкие ссадины. Клинические проявления (локализованная флегмона, болезненные узелки или абсцесс со свищевым ходом), как правило, возникают через 4-6 нед. Описан единственный случай мастита, вызванного М. abscessus, обусловленного пирсингом соска молочной железы. М. haemophilum служит причиной болезненных подкожных узелков у больных с иммуносупрессией (особенно после трансплантации почки); эти узелки часто изъязвляются и нагнаиваются.
Среди возбудителей инфекций, связанных с венозными катетерами, доля атипичных микобактерий невелика, однако она растет. Такие инфекции представляют собой бактериемию или нагноение по ходу установки катетера; основную роль в них играют М. fortuitum, М. chelonae и М. abscessus.
У взрослых атипичные микобактерии чаще всего поражают органы дыхания, однако для детей это нетипично. Тем не менее у детей с нормальным иммунитетом описаны вызванные комплексом М. aviumострые пневмонии, длительный кашель или свистящее дыхание вследствие сдавления дыхательных путей увеличенными паратрахеальными или парабронхиальными лимфатических узлами. Описаны также единичные случаи прогрессирования инфекции с гранулематозным воспалением бронхов. У больных старшего возраста с муковисцидозом возбудителями хронических инфекций могут быть микобактерии комплекса М. avium и комплекса М. fortuitum. У взрослых с хроническими заболеваниями легких инфекции вызывают М. kansasii, М. xenopi и М. szulgai; у детей эти возбудители нетипичны. Заболевание начинается постепенно с субфебрильной температуры тела, кашля, ночной потливости и общего недомогания. Характерно формирование тонкостенных каверн, инфильтрация паренхимы вокруг которых выражена минимально; иногда рентгенологическая картина напоминает туберкулез.
Изредка, обычно у больных с операционными или колотыми ранами, атипичные микобактерии могут вызывать инфекции костей и суставов, неотличимые от обусловленных М. tuberculosis и другими бактериями. У больных с колотыми ранами стоп М. fortuitum вызывает инфекции, напоминающие вызванные Pseudomonas aeruginosa или Staphylococcus aureus.
Атипичные микобактерии, обычно относящиеся к комплексу М. avium, изредка вызывают диссеминированную инфекцию без видимых признаков иммунодефицита. У большинства детей обнаруживаются мутации генов, которые кодируют рецепторы ИФН-у или ИЛ-12, либо образование ИЛ-12. При отсутствии рецепторов к ИФН-у развивается тяжелая инфекция, которую трудно лечить. Инфекции у детей с дефицитом рецепторов к ИФН-у или мутациями генов, которые участвуют в синтезе ИЛ-12, протекают легче и поддаются лечению интерфероном и антимикобактериальными средствами. Частота многоочагового остеомиелита наиболее высока у детей с мутацией рецептора-1 ИФН-у 818del4. Имеются многочисленные описания рецидивов, возникающих через годы после лечения.
Диссеминированная инфекция комплексом М. avium, одна из частых оппортунистических инфекций, особенно на поздних стадиях СПИДа, когда число СD4-лимфоцитов падает ниже 100/мм3. Диссеминированной инфекции, по всей видимости, предшествует колонизация дыхательных путей или ЖКТ комплексом М. avium. Но исследование секрета дыхательных путей или кала на данный возбудитель не позволяет предсказать возможность диссеминации. Для диссеминированной инфекции типичны длительная бактериемия с высоким содержанием возбудителей в крови и поражение множества органов, в первую очередь лимфатических узлов, печени, селезенки, костного мозга и ЖКТ. Также могут вовлекаться щитовидная и поджелудочная железы, надпочечники, почки, мышцы и головной мозг. Самыми частыми симптомами диссеминированной инфекции при СПИДе, вызванной комплексом М. avium, служат лихорадка с ознобами, ночная потливость, потеря аппетита, выраженное похудение, слабость, генерализованная лимфаденопатия и гепатоспленомегалия. Возможны также желтуха, повышение активности щелочной фосфатазы, и нейтропения. Лучевые исследования обычно демонстрируют выраженное увеличение лимфоузлов корней легких, средостения, брыжейки и забрюшинных лимфатических узлов. Средняя продолжительность жизни у больных СПИДом детей после высевания комплекса М. avium из крови или тканей составляет 5-9 мес.
Диагностика атипичных микобактерий
Дифференциальная диагностика лимфаденита от атипичных микобактерий, включает острый бактериальный лимфаденит, туберкулезный лимфаденит, фелиноз (возбудитель - Bartonella henselae),мононуклеоз, токсоплазмоз, бруцеллез, туляремию и злокачественные опухоли, в первую очередь лимфомы. Проба Манту с 5 туберкулиновыми единицами обычно слабо положительна (инфильтрат диаметром 5-15 мм). В Центре по контролю заболеваемости были созданы антигены для кожных проб, которые позволяют различить микобактерии, относящиеся к разным группам по Раньону, однако эти антигены более не выпускаются. Инфекции атипичными микобактериями бывает трудно отличить от туберкулеза. Но при лимфадените от атипичных микобактерий, диаметр инфильтрата при пробе Манту обычно не достигает 15 мм, увеличиваются передние шейные лимфатические узлы с одной стороны, рентгенограммы грудной клетки в норме, контакт с взрослым больным туберкулезом отсутствует. При туберкулезном лимфадените, как правило, имеется двустороннее увеличение задних шейных лимфатических узлов, диаметр инфильтрата при пробе Манту превышает 15 мм, при рентгенографии грудной клетки обнаруживается патология, а также удается выявить контакт с взрослым больным туберкулезом. Окончательный диагноз ставят после удаления пораженных лимфатических узлов и посева.
Диагностика кожных микобактериальных инфекций основана на посеве биоптата из очага поражения. Диагностика инфекции органов дыхания, вызванных атипичными микобактериями, затруднена, поскольку многие из атипичных микобактерий, включая комплекс М. avium, могут высеваться из секрета полости рта и желудка у здоровых детей. Для окончательной диагностики требуются инвазивные исследования, например бронхоскопия с биопсией бронха или легкого. Миколевые кислоты и другие липиды, содержащиеся в клеточной стенке микобактерий, придают им кислотоустойчивость при окраске по Цилю-Нельсену или Киньуну. Микобактерии также можно выявить путем окраски флюоресцентными красителями, такими какаурамин и родамин. Чувствительность окраски атипичных микобактерий в тканях ниже, чем при обнаружении М. tuberculosis.
Чувствительность посева крови у больных СПИДом с диссеминированной инфекцией атипичными микобактериями, достигает 90-95 %. Посев крови на специальные среды, в которых используется радиометрический метод, позволяет в течение недели обнаружить комплекс М. avium практически у всех больных. Выпускаются также ДНК-зонды, с помощью которых удается различить атипичные микобактерии и М. tuberculosis. Быстрый метод предварительной диагностики диссеминированной микобактериальной инфекции - это обнаружение в костном мозге и биоптатах других тканей гистиоцитов, содержащих множество кислотоустойчивых палочек.
Лечение атипичных микобактерий
При инфекциях атипичными микобактериями, используется как консервативное, так хирургическое лечение, а также их комбинация. Лучше всего, если удается выделить возбудитель и определить его чувствительность, потому что последняя варьирует. М. kansasii, М. xenopi, М. ulceransи М. malmoense обычно чувствительны к стандартным противотуберкулезным средствам. М. fortuitum, М. chelonae, М. scrofulaceum и комплекс М. avium к противотуберкулезным средствам в большинстве случаев устойчивы; чувствительность их к новым антибактериальным средствам, таким как фторхинолоны и макролиды, непостоянна. Чтобы избежать развития устойчивости, необходимо назначать несколько антибактериальных средств одновременно.
Предпочтительный метод лечения атипичного лимфаденита, - полное иссечение пораженных лимфатических узлов. Лимфоузлы удаляют, пока они еще плотные и капсула их цела. Развитие обширного казенного некроза с переходом на окружающие ткани затрудняет иссечение, а также повышает вероятность осложнений (повреждение лицевого нерва, рецидив инфекции). Не следует удалять только часть лимфатических узлов, так как в этом случае может возникнуть длительно незаживающий свищ. Стандартные противотуберкулезные средства при лимфадените, вызванном атипичными микобактериями, малоэффективны, а полное иссечение лимфатических узлов делает их ненужными. Если же туберкулез исключить нельзя, назначают изониазид, рифампицин и пиразинамид до получения результатов посева. Если по тем или иным причинам иссечь пораженные лимфатические узлы невозможно, либо их иссечение было неполным, либо возник рецидив или свищ, рекомендуется медикаментозное лечение продолжительностью 4-6 мес. Хотя нет опубликованных данных контролируемых исследований, ряд наблюдений и мелкие исследования свидетельствуют об успешном применение только медикаментозного лечения или его комбинации с удалением лимфоузлов. Согласно большинству сообщений, использовался кларитромицин или азитромицин с рифабутином или этамбутолом.
Инфекции кожи, вызванные микобактериями, после обычно заживают самостоятельно. М. marinum чувствительна к рифампицину, амикацину, этамбутолу, сульфаниламидам, триметоприм/сульфаметоксазолу и тетрациклину. Комбинацию перечисленных препаратов назначают на 3-4 мес. Инъекции глюкокортикоидов противопоказаны. Поверхностные инфекции, возбудителями которых служат М. fortuitum и М. chelonae, обычно заживают после открытого дренирования. При глубоких инфекциях, а также при инфекциях, связанных с венозными катетерами, необходимо удалить катетер и начать парентеральное введение амикацина, цефокситина или кларитромицина. При инфекциях органов дыхания до получения результатов исследования чувствительности назначают комбинацию изониазида, рифампицина и пиразинамида.
При диссеминированной инфекции комплексом М. avium, больным с нарушениями синтеза ИЛ-12 или дефицитом рецепторов ИФН-у показана комбинация кларитромицина либо азитромицина с одним или более из следующих препаратов: рифабутин, клофазимин, этамбутол и фторхинолоны. Лечение продолжают не менее 12 мес. Важное значение имеет определение чувствительности возбудителя in vitro. После окончания лечения рекомендуется пожизненная профилактика рецидивов, для чего назначают ежедневный прием кларитромицина. Наличие специфических генетических дефектов служит показанием к назначению интерферона.
У взрослых больных СПИДом ежедневный профилактический прием азитромицина или его комбинации с рифабутином снижает частоту инфекций, вызванных комплексом М. avium, больше чем на 50 %.
Статью подготовил и отредактировал: врач-хирургМ. tuberculosis - М. туберкулеза человека (М. tuberculosis Lehmann, Neumann 1896; син.: М. tuberculosis typus humanus Lehmann, Neumann 1907, M. tuberculosis var. hominis Bergey 1934). В Определителе бактерий Берджи (1974) представлено описание штамма Н37 Rv. Строго кислото- и щелочеустойчив. Рост медленный при t° 37°, возможен при t° 30-34°. Оптимум pH 6,4-7,0. Более обильный и быстрый рост на средах с глицерином. Вызывает редукцию нитратов, ниацинположителен, каталазная активность теряется при нагревании до t° 68°. М. tuberculosis вызывает туберкулез у человека и человекообразных обезьян, а также у животных, контактирующих с человеком.
Доза возбудителя 0,01 мг высокопатогенна для морских свинок II хомяков, менее патогенна для кроликов, кошек, коз, рогатого скота и домашних птиц. Для заражения мышей используют дозы возбудителя 0,001 - 1 мг. От больных туберкулезной волчанкой и мочеполовым туберкулезом выделяются М. с более низкой вирулентностью. Инфицированные животные, а также человек проявляют замедленную гиперчувствительность к туберкулину, полученному из возбудителей туберкулеза, и меньшую чувствительность к туберкулиновым препаратам из других видов М.- сенситинам. Антигенная структура М. tuberculosis близка к М. bovis, М. microti и М. kansasii.
М. bovis- М. туберкулеза рогатого скота (М. bovis Karlson, Lessel 1970); син.: M. tuberculosis typus bovinus Lehmann, Neumann 1907, M. tuberculosis var. bovis Bergey et al. 1934). Первично-изолированные культуры слабо растут на средах с глицерином, колонии без пигментов, тест на ниацин отрицательный. Штаммы, устойчивые к изониазиду, лишены каталазной активности, нек-рые из них устойчивы к парааминосалициловой к-те. Вызывают туберкулез у рогатого скота, людей» плотоядных животных, свиней, попугаев и нек-рых хищных птиц. Высокопатогенны для кроликов, морских свинок, телят; умеренно патогенны для хомяков и мышей; слабопатогенны для собак, кошек, лошадей и крыс; непатогенны для большинства птиц. Нек-рые штаммы, изолированные от больных волчанкой и скрофулодермой, обладают низкой патогенностью для животных. Туберкулины, приготовленные из М. tuberculosis и М. bovis, практически одинаковы по своему действию. Бактерии Кальметта-Герена (BCG) обладают теми же свойствами, что и М. bovis, однако более аттенуированы и хорошо растут на средах с глицерином.
М. microti - М. мышей-полевок (М. microti Beed 1957; син.: М. tuberculosis var. muris Brooke 1941, Vole bacillus Wells 1937). Растут на глицериновых средах при t° 37° в течение 28-60 дней. Вызывают генерализованный туберкулез у полевок, местные поражения у морских свинок, кроликов, телят. По иммунол, признакам наиболее близки к М. tuberculosis и М. bovis.
М. paratuberculosis - М. паратуберкулеза рогатого скота (М. paratuberculosis Bergey et al. 1923, син. Johne’s bacillus). Требуют специальных факторов роста. Впервые удалось получить рост на средах с убитыми кислотоустойчивыми бактериями. Культивируют также на синтетических средах. Вызывают гипертрофический энтерит у рогатого скота. Непатогенны для морских свинок, крыс, мышей; только в очень больших дозах могут вызывать у них незначительные местные узелковые поражения. Имеют четыре антигена, общих с М. avium, и пять - с М. tuberculosis.
М. africanum - микобактерии африканум (М. africanum Castets, Rist, Boisvert 1969). Растут при t° 37° на яичных и агаровых средах с бычьей сывороткой. Выделяются от больных туберкулезом в тропической Африке. Патогенны для морских свинок, мышей и отчасти кроликов.
М. lepraemurium - М. лепры крыс (М. leprae murium Marchoux, Sorel 1912). He растут на питательных средах, в эксперименте перевиваются крысам, мышам, хомякам. Вызывают эндемию среди крыс и кожные узелковые поражения у других животных.
В природе существует обширная группа условно-патогенных М., к-рые вызывают микобактериозы. Специфическая терапия туберкулеза и микобактериозов различна, в связи с чем особое значение имеет идентификация возбудителя. Если для целей таксономии и выявления генетических связей между представителями рода М. предложено более 100 тестов и их комплексов, то для практического использования удобен вариант классификации, разработанный Раньоном (Е. Runyon, 1959, 1965). Условно-патогенные и сапрофитные М., названные автором атипичными, делятся на 4 группы по ограниченному числу признаков - скорости роста, пигментообразовании, морфологии колоний, нек-рым культурально-биохим. показателям.
Группа I - фотохромогенные: М. kansasii, var. luciflavum, var. aurancicum, var. album. Главный признак - появление пигмента на свету. Колонии от S- до RS-формы, содержат кристаллы каротина, окрашивающие их в желтый цвет; имеются культуры, лишенные пигмента. Скорость роста от 7 до 20 дней при t° 37°; обычно строго каталазопозитивны. Выделяются от людей с поражениями легких, похожими на туберкулез.
Группа II - скотохромогенные: М. marianum, М. aqua, М. flavescens.
Кислотоустойчивые палочки; образуют в темноте желтые, а на свету оранжевые или красноватые колонии, обычно S-формы; рост медленный при t° 37°. Скотохромо генные условно-патогенные виды М. gordonae и М. scrofulaceum по указанным признакам близки к сапрофитам этой группы - М. flavescens и М. aqua, отличаются от них по устойчивости к 5% р-ру NaCl, гидролизу твин-80, редукции нитратов. Патогенность для человека и лаб. животных незначительна. Иногда вызывают лимфадениты у детей. Выделяются из загрязненных водоемов, почвы.
Группа III - нехромогенные: М. avium (intracellulare, battey, Bataglini ulcerans), M. gastri, М. terrae, М. xenopi. Кислотоустойчивые палочки, колонии S- или SR- и R-формы; обычно бесцветные. М. avium и М. intracellulare различают по серологическим признакам; в этом комплексе насчитывается 23 серотипа. М. avium дают отрицательный тест на арилсульфатозу, у М. intracellulare и других представителей этой группы он положителен. Условно-патогенные виды отличаются от сапрофитов по устойчивости к 5% р-ру хлорида натрия и гидролизу твина-80. Патогенны для птиц, менее патогенны для рогатого скота, свиней, овец, собак. Выделяются от больных животных, из воды и почвы.
Группа IV - быстрорастущие: М. marinum, М. fortuitum, М. phlei, М. smegmatis, М. borstelense, М. vaccae, М. thamnopheos. Рост от 1-2 до 14 дней, возможен при t° выше 45° (М. smegmatis), колонии R- или S-формы. Скотохромогенные и фотохромогенные штаммы этой группы редко выделяются из патол, материала больных, однако нек-рые из них имеют клин, значение.
Роль атипичных М. как возбудителей заболеваний стала известна в начале века. В разных р-нах мира выделение их от людей колеблется от нескольких случаев до 20-42% (М. П. Зыков, 1966, и др.). Ок. 1/3 микобактериозов вызывают М. kansasii (I группа), затем М. avium и М. intracellulare (III группа) и представители IV группы (М. fortuitum, М. borstelense и др.). Наименьшее патогенетическое значение имеет II группа. Нетуберкулезные М. могут выделяться от здоровых лиц и от больных туберкулезом. Для диагностики микобактериозов, а также изучения инфицированности населения условно-патогенными М. применяют аллергические пробы С сенситинами. В связи с устойчивостью многих М. к антибиотикам и другим лекарственным веществам использование для идентификации штаммов этого критерия считается мало надежным, так же как и тестов на вирулентность для лаб. животных.
Библиография: Зыков М. П. и Ильина Т. Б. Потенциально-патогенные микобактерии и лабораторная диагностика микобактериозов, М., 1978, библиогр.; Лазовская А. Л. и Блохина И. Н. Патогенные и условно-патогенные микобактерии, Горький, 1976, библиогр.; Яблокова Т. Б. и др. Оценка диагностического значения сенситинов в эксперименте и клинике, Пробл, туб., № 7, с. 62, 1977, библиогр.; A typical mycobacteria, ed. by J. G. Weiszfeiler, Budapest, 1973; Bergey’s manual of determinative bacteriology, ed. by R. E. Buchanan a. N. E. Gibbons, Baltimore, 1975; R u-n у o n Е.Н. Typical mycobacteria, Their classification, Amer. Rev. resp. Dis., v. 91, p. 288, 1965.
Т. Б. Яблокова.
Mycobacterium
Lehmann and
Neumann
| Систематика на Викивидах | Изображения на Викискладе |
|
Уникальность и ключевая роль миколовых кислот в структурной организации и физиологии микобактерий делают их отличной мишенью для этиотропной терапии .
Размножаются делением клеток. Широко распространены в почве. Сапрофитные формы участвуют в минерализации органических остатков, некоторые окисляют парафины и другие углеводороды. Могут использоваться для борьбы с загрязнением биосферы нефтью .
Пигментация
Согласно классификации Раньона нетуберкулёзных микобактерий на основе культуральных различий от 1959 года , по продукции пигмента колониями выделяют 4 группы микобактерий:
Фотохромогенные (Группа I) Микобактерии, непигментированные при выращивании в темноте, но приобретающие ярко-жёлтую или жёлто-оранжевую пигментацию после выдерживания или реинкубации на свету.
- Ex: M. kansasii , M. marinum , M. simiae , M. asiaticum
- Ex: M. scrofulaceum , M. gordonae , M. xenopi , M. szulgai
- Ex: M. tuberculosis , M. avium , M.intra-cellulare , M. bovis , M. ulcerans
- Ex: M. chelonae
- Ex: M. phlei , M. smegmatis , M. fortuitum
Патогенные виды
Патогенные виды вызывают болезни человека (туберкулёз , лепру , микобактериозы) и животных. Всего известно 74 вида таких микобактерий. Они широко распространены в почве, воде и среди людей.
Туберкулёз у человека вызывают виды : Mycobacterium tuberculosis typus (человеческий вид), Mycobacterium bovis (бычий вид) и Mycobacterium africanum (промежуточный вид), у больных СПИД - также виды Mycobacterium avium complex . Эти виды способны проникать, жить и размножаться внутри человека.
Представители рода микобактерий
По старой системе микобактерии классифицировались, в зависимости от их свойств и скорости роста на питательных средах. Однако более новая номенклатура базируется на кладистике .
Медленно растущие
Микобактерии туберкулёзного комплекса (MTBC)
- Mycobacterium tuberculosis complex (MTBC) представители комплекса патогенны для человека и животных, и вызывают заболевание туберкулёз . Комплекс включает: M. tuberculosis , наиболее опасен для человека, как возбудитель туберкулёза M. bovis M. bovis BCG M. africanum M. canetti M. caprae M. microti M. pinnipedii
Микобактерии avium-комплекса (MAC)
Mycobacterium avium complex (MAC) - часть большой группы нетуберкулёзных микобактерий (НТМБ), виды, составляющие данный комплекс, патогенны для человека и животных, чаще вызывают диссеминированные процессы внелёгочной локализации и являлись ранее одной из основных причин смерти больных СПИДом . Комплекс включает:
- M. avium M. avium paratuberculosis M. avium silvaticum M. avium «hominissuis» M. colombiense
Gordonae-ветвь
- M. asiaticum
- M. gordonae
Kansasii-ветвь
- M. gastri
Нехромогенные/terrae-ветвь
- M. hiberniae
- M. nonchromogenicum
- M. terrae
- M. triviale
Микобактерии, продуцирующие миколактон
- M. ulcerans
- M. pseudoshottsii
- M. shottsii
Simiae-ветвь
- M. triplex
- M. genavense
- M. florentinum
- M. lentiflavum
- M. palustre
- M. kubicae
- M. parascrofulaceum
- M. heidelbergense
- M. interjectum
- M. simiae
Некатегоризированные
- M. branderi
- M. cookii
- M. celatum
- M. bohemicum
- M. haemophilum
Быстро растущие
Сhelonae-ветвь
- M. abscessus
- M. chelonae
- M. bolletii
Fortuitum-ветвь
- M. fortuitum
- M. fortuitum subsp. acetamidolyticum
- M. boenickei
- M. peregrinum
- M. porcinum
- M. senegalense
- M. septicum
- M. neworleansense
- M. houstonense
- M. mucogenicum
- M. mageritense
- M. brisbanense
- M. cosmeticum
Parafortuitum-ветвь
- M. parafortuitum
- M. austroafricanum
- M. diernhoferi
- M. hodleri
- M. neoaurum
- M. frederiksbergense
Vaccae-ветвь
- M. aurum
- M. vaccae
CF-ветвь
- M. chitae
- M. fallax
Некатегоризированные
- M. confluentis
- M. flavescens
- M. madagascariense
- M. phlei
- M. smegmatis
- M. goodii
- M. wolinskyi
- M. thermoresistibile
- M. gadium
- M. komossense
- M. obuense
- M. sphagni
- M. agri
- M. aichiense
- M. alvei
- M. arupense
- M. brumae
- M. canariasense
- M. chubuense
- M. conceptionense
- M. duvalii
- M. elephantis
- M. gilvum
- M. hassiacum
- M. holsaticum
- M. immunogenum
- M. massiliense
- M. moriokaense
- M. psychrotolerans
- M. pyrenivorans
- M. vanbaalenii
Нетуберкулезные микобактерии - самостоятельные виды, широко распространенные в окружающей среде, как сапрофиты, которые в некоторых случаях могут вызывать тяжело протекающие заболевания - микобактериозы. Их также называют микобактериями окружающей среды (environmental micabacteria), возбудителями микобактериозов, оппортунистическими и атипичными микобактериями. Существенным отличием нетуберкулезных микобактерий от микобактерии туберкулезного комплекса является то, что они практически не передаются от человека к человеку.
Нетуберкулезные микобактерии делятся на 4 гуппы по ограниченному числу признаков: скорости роста, образованию пигмента, морфологии колоний и биохимическим свойствам.
1-я группа - медленнорастущие фотохромогенные (М. kansasii и др.). Главный признак представителей этой группы появление пигмента на свету. Они образуют колонии от S до RS-форм, содержат кристаллы каротина, окрашивающие их в желтый цвет. Скорость роста от 7 до 20 дней при 25, 37 и 40 °С, катадазоположительны.
М. kansasii - желтые бациллы, обитают в воде, почве, чаще всего поражают легкие. Эти бактерии можно идентифицировать за счет их больших размеров и крестообразного расположении. Важным проявлением инфекций, вызванных М. kansasii, считается развитие диссеминированного заболевания. Возможны также поражения кожи и мягких тканей, развитие теносиновитов, остеомиелита, лимфаденитов, перикардитов и инфекций органов мочеполового тракта .
2-я группа - медленнорастущие скотохромогенные (М. scrofulaceum, М. matmoense, M. gordonae и др.). Микроорганизмы образуют II темноте желтые, а па свету оранжевые или красноватые колонии, обычно S-формы колоний, растут при 37 °С. Это самая многочисленная группа нетуберкулезных микобактерий. Они выделяются из загрязненных водоемов и почвы а обладают незначительной патогенностью для человека и животных.
М. scrofulaceum (от англ. scrofula - золотуха) - одна из основных причин развития шейного лимфаденита у детей до 5 лет. При наличии тяжелых сопутствующих заболеваний они могут вызвать поражения легких, костей и мягких тканей. Помимо воды и почвы, микробы выделены из сырого молока и других молочных продуктов.
М. maimoense - микроаэрофилы, образуют серовато-белые гладкие блестящие непрозрачные куполообразные круглые колонии.
Первичные изоляты растут очень медленно при 22-37 °С. Экспозиция их на свету не вызывает продукции пигмента, В случае необходимости экспозиции продолжают до 12 нед. У человека они вызывают хронические заболевания легких.
М. gordonae - самые распространенные общепризнанные сапрофиты, скотохромогены водопроподной воды, микобактериоз вызывают крайне редко. Помимо воды (известны как М. aquae) их часто выделяют из почвы, промывных вод желудка, бронхиального секрета или другого материала от больных, но в большинстве случаев они оказываются непатогенными для человека. В то же время имеются сообщения о случаях менингита, перитонита и кожных поражений, вызванных этим видом микобактерий.
3-я группа - медленнорастущие нехромогенные микобактерии (М. avium complex, M. gaslri M. terrae complex и др.). Они образуют бесцветные S- или SR- и R-фор мы колоний, которые могут иметь светло-желтые и кремовые оттенки. Выделяются от больных животных, из воды и почвы.
М. avium - М. inlracellulare объединены в один М. avium complex так как их межвидовая дифференциация представляет определенные трудности. Микроорганизмы растут при 25-45 °С, патогенны для птиц, менее патогенны для крупного рогатого скота, свиней, овец, собак и не патогенны для морских свинок. Наиболее часто эти микроорганизмы вызывают у человека поражения легких. Описаны поражения кожных покровов, мышечной ткани и костного скелета, а также диссеминированные формы заболеваний. Они входят в число возбудителей оппортунистических инфекций, осложняющих синдром приобретенного иммунодефицита (СПИД). М. avium подвид paratuberculosis является возбудителем болезни Джонса у крупного рогатого скота и, возможно, болезни Крона (хроническое воспалительное заболевание желудочно-кишечного тракта) у человека. Микроб присутствует в мясе, молоке и фекалиях инфицированных коров, а также обнаруживается в воде и почве. Стандартные методы очистки воды не инактивируют данный микроб.
М. xenopi вызывает поражения легких у человека и диссеминированные формы заболеваний, связанные со СПИДом. Они выделены от лягушек рода Xenopus. Бактерии образуют мелкие с гладкой блестящей поверхностью не пигментированные колонии, которые в последующем окрашиваются в ярко-желтый цвет. Термофилы не растут при 22 °С и дают хороший рост при 37 и 45 °С. При бактериоскопии выглядят как очень тонкие палочки, суживающиеся с одного конца и расположенные параллельно друг другу (и виде частокола). Часто выделяются из холодной и горячей водопроводной воды, включая воду для питья, хранящуюся в больничных резервуарах (нозокомиальные вспышки). В отличие от других условно-патогенных микобактерий они чувствительны к действию большинства противотуберкулезных препаратов.
М. ukerans - этиологический агент микобактериальной кожной N (язва Бурули), растет только при 30-33 °С, Рост колоний отмечается лишь через 7 нед. Выделение возбудителя происходят также при заражении мышей в мякоть подошвы лапки. Данное заболевание распространено в Австралия и Африке. Источником инфекции служит тропическое окружение и вакцинация БЦЖ вакциной от этого микобактериоза.
4-я группа - быстрорастущие микобактерий (М. fortuitum complex, M. phlei, М. xmegmatis и др.). Рост их отмечается в виде R- или S-форм колоний в течение от 1-2 до 7 дней. Они обнаруживаются в воде, почве, нечистотах и являются представителями нормальной микрофлоры тела человека. Бактерии этой группы редко выделяются из патологического материала от больных, однако некоторые из них имеют клиническое значение.
М. fortuitum complex включает М. fortuitum и М. chcionae, которые состоят из подвидов. Они вызывают диссеминированные процессы, кожные и послеоперационные инфекции, заболевания легких. Микробы данного комплекса высокоустойчивы к противотуберкулезным препаратам.
М smegmatis - представитель нормальной микрофлоры, выделяется из смегмы у мужчин. Хорошо растет при 45 °С. Как возбудитель заболеваний человека занимает второе место среди быстрорастущих микобактерий после комплекса М. fortuitum. Поражает кожу и мягкие ткани. Возбудителей туберкулеза необходимо дифференцировать от М. smegmatis при исследовании мочи.
Эпидемиология микобактериозов
Возбудители микобактериозов широко распространены в природе. Их можно обнаружить в почве, пыли, торфе, грязи, воде рек, водоемов и плавательных бассейнов. Они обнаруживаются у клещей и рыб, вызывают заболевания у птиц, диких и домашних животных, являются представителями нормальной микрофлоры слизистых оболочек верхних дыхательных путей и мочеполового тракта у человека. Заражение нетуберкулезными микобактериями происходит из окружающей среды аэрогенно, контактным путем при повреждении кожных покровов, а также пищевым и водным путями. Передача микроорганизмов от человека к человеку нехарактерна. Это условно-патогенные бактерии, поэтому большое значение в возникновении заболевания имеют снижение резистентности макроорганизма, его генетическая предрасположенность. В пораженных участках образуются гранулемы. В тяжело протекающих случаях фагоцитоз носит незавершенный характер, бактериемия выражена, а в органах определяются макрофаги, заполненные нетуберкулезные микобактерии и напоминающие лепрозные клетки.
, , , , , , , ,
Симптомы микобактериозов
Симптомы микобактериозов разнообразны. Чаще всего поражается дыхательная система. Симптоматика легочной патологии сходна с таковой при туберкулезе. Вместе с тем нередки случаи внелегочной локализации процесса с вовлечением кожи и подкожной клетчатки, раневых поверхностей, лимфатических узлов, мочеполовых органов, костей и суставов, а также мозговых оболочек. Органные поражения могут начинаться как остро, так и скрыто, но почти всегда протекают тяжело,
Возможно также развитие смешанной инфекции (mixt-инфекции), в ряде случаев они могут быть причиной развития вторичной эндогенной инфекции.
Микробиологическая диагностика микобактериозов
Основной метод диагностики микобактериозов бактериологический. Материал на исследование берут, исходя из патогенеза и клинических проявлений заболевания. Первоначально решается вопрос о принадлежности выделенной чистой культуры к возбудителям туберкулеза или нетуберкулезным микобактериям. Затем применяют комплекс исследований, позволяющих установить вид микобактерий, степень вирулентности, а также группу по Раньону. Первичная идентификация основана на таких признаках, как скорость роста, способность к образованию пигмента, морфология колоний и способность роста при различных температурах. Для выявления этих признаков не требуется дополнительного оборудования и реактивов, поэтому они могут применяться в базовых лабораториях противотуберкулезных диспансеров. Окончательная идентификация (референс-идентификация) с применением сложных биохимических исследований проводится в специализированных мораториях научных учреждений. В большинстве случаев предпочтение отдают их идентификации по биохимическим фактам таким, как современные молекулярно-генетические методы трудоемк, имеют много подготовительных стадий, требуют специального оборудования, дорогостоящие. Большое значение для печения имеет определение чувствительности к антибиотикам. Решающее значение для постановки диагноза микобактериоза имеет критерий одновременности появления клинических, рентгенологических, лабораторных данных и выделения чистой культуры нетуберкулезных микобактериий, проведение многократных исследований в динамике.